-
GB/T 14926.14-2001 实验动物 金黄色葡萄球菌检测方法
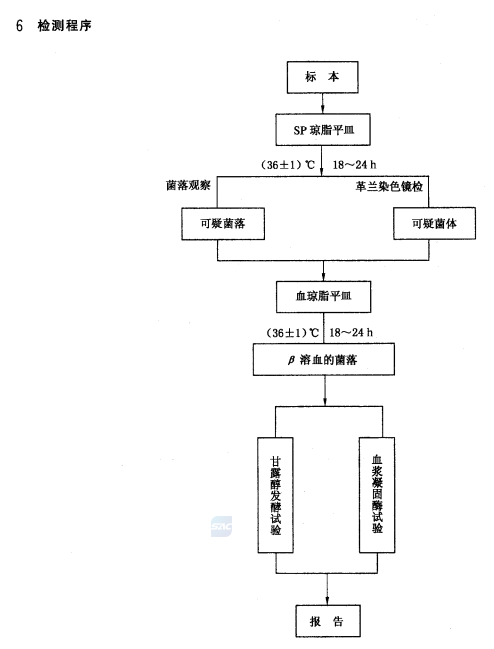
本标准规定了实验动物金黄色葡萄球菌的检测方法。本标准适用于小鼠、大鼠、豚鼠、地鼠和免金黄色葡萄球菌的检测
大小:298.71KB 更新时间: 2025-07-11 安全下载 -
GB/T 14926.13-2001 实验动物 肺炎克雷伯杆菌检测方法
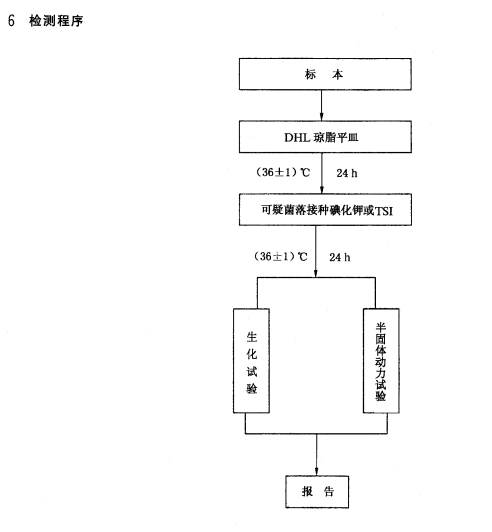
范围本标准规定了实验动物肺炎克雷伯杆菌的检测方法。本标准适用于小鼠、大鼠、豚鼠、地鼠、免肺炎克雷伯杆菌的检测。2引用标准...
大小:296.89KB 更新时间: 2025-07-11 安全下载 -
GB/T 14926.12-2001 实验动物 嗜肺巴斯德杆菌检测方法

本标准规定了实验动物嗜肺巴斯德杆菌的检测方法。本标准适用于小鼠、大鼠、豚鼠、地鼠和兔嗜肺巴斯德杆菌的检测。引用标准下列标...
大小:314.41KB 更新时间: 2025-07-11 安全下载 -
药物涂层球囊扩张导管注册审查指导原则(2023年第9号)

本指导原则旨在指导注册申请人对药物涂层球囊扩张导管注册申报资料的准备及撰写,同时也为技术审评部门对药物涂层球囊扩张导管注...
大小:63.75KB 更新时间: 2025-02-23 安全下载 -
主动脉覆膜支架系统临床试验指导原则(2019年第8号)

为了进一步规范主动脉覆膜支架系统产品上市前的临床试验,并指导该类产品申请人在申请产品注册时临床试验资料的准备,制订本指导...
大小:42.5KB 更新时间: 2025-02-23 安全下载 -
YY/T 1859-2022 动物源性心血管植入物抗钙化评价 大鼠皮下植入试验

本文件按照 GB/T 1.1-2020《标准化工作导则第1部分:标准化文件的结构和起草规则》的规定起草。 请注意本文件的...
大小:3.23MB 更新时间: 2025-02-23 安全下载 -
生物可吸收冠状动脉药物洗脱支架动物实验研究指导原则(2020年第48号)

为了进一步规范生物可吸收冠状动脉药物洗脱支架(下简称生物可吸收支架)产品动物实验研究,并指导该类产品注册申请人在申请产品...
大小:37KB 更新时间: 2025-02-23 安全下载 -
生物可吸收冠状动脉药物洗脱支架临床试验指导原则(2019年第8号)

为了进一步规范生物可吸收冠状动脉药物洗脱支架产品上市前的临床试验,并指导该类产品申请人在申请产品注册时临床试验资料的准备...
大小:39KB 更新时间: 2025-02-23 安全下载 -
冠状动脉药物洗脱支架临床试验指导原则(2018年第21号)

为了进一步规范冠状动脉药物洗脱支架产品上市前的临床试验,并指导该类产品申请人在申请产品注册时临床试验资料的准备,制订本指...
大小:68.5KB 更新时间: 2025-02-23 安全下载 -
YY 0315-2023 钛及钛合金牙种植体

本文件按照 GB/T 1.1-2020《标准化工作导则 第1部分:标准化文件的结构和起草规则》的规定起草。 本文件代替 ...
大小:4.47MB 更新时间: 2025-02-22 安全下载



