近日,中国科学院水生生物研究所胡炜研究员团队与加拿大渥太华大学Vance L. Trudeau教授团队合作,在 Science China Life Sciences 发表了题为"Olfactory GnRH3 crypt sensory neurons transduce sex pheromone signals to induce male courtship behavior in zebrafish"的封面论文。该研究发现斑马鱼嗅觉上皮中的GnRH3神经元是一种隐窝嗅觉感觉神经元(Crypt Olfactory Sensory Neuron),可直接感知性信息素PGF2α,并触发雄性求偶行为,为阐释脊椎动物嗅觉感知和生殖行为的神经机制提供了新见解。
嗅觉上皮是脊椎动物感知嗅觉信号的初级器官,大量的嗅觉感觉神经元在此处聚集,但是至今未见GnRH神经元在嗅觉上皮上分布的研究报道。过去30多年来,脊椎动物下丘脑外末端GnRH神经元一直被认为起源于嗅基板(Olfactory Placode),并以单向方式从嗅基板迁移到下丘脑。但研究团队发现,斑马鱼下丘脑外末端GnRH神经元(即GnRH3神经元)起源于嗅基板腹侧基底部(视频1)。随着斑马鱼胚胎的发育,GnRH3神经元会同时向前后两个方向分离并迁移细胞。向后迁移出的GnRH3神经元定位到下丘脑,发挥经典的生殖调控功能。向前迁移的GnRH3神经元细胞最终分布在嗅觉上皮(Olfactory Epithelium, OE),是一种表达嗅觉受体ora4的隐窝嗅觉感觉神经元(Crypt Olfactory Sensory Neuron),发挥感知和传递性信息素PGF2α的嗅觉感知功能,属于尚未被认知的GnRH3神经元新亚群,研究团队将这一GnRH3神经元新亚群定义为GnRH3-OE(图1,图2),从而在脊椎动物嗅觉上皮中发现了GnRH神经元细胞体的分布。
继续观看
ZebrafishAdvance | 胡炜团队发现嗅觉调控斑马鱼求偶行为的神经机制
观看更多转载,ZebrafishAdvance | 胡炜团队发现嗅觉调控斑马鱼求偶行为的神经机制中国斑马鱼信息中心已关注分享点赞在看已同步到看一看写下你的评论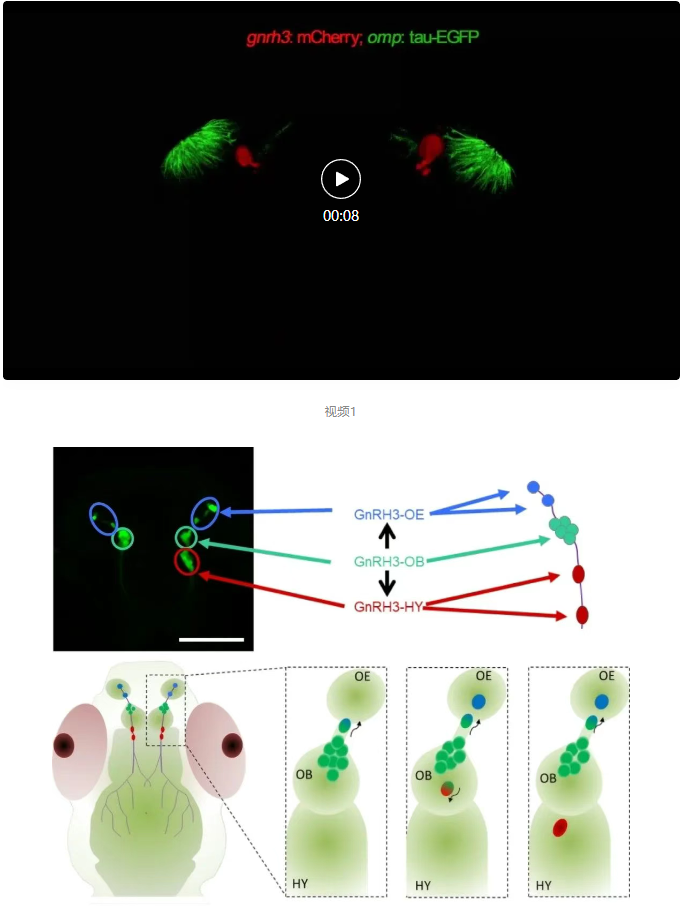
图1 斑马鱼GnRH3神经元迁移和分布的新模式
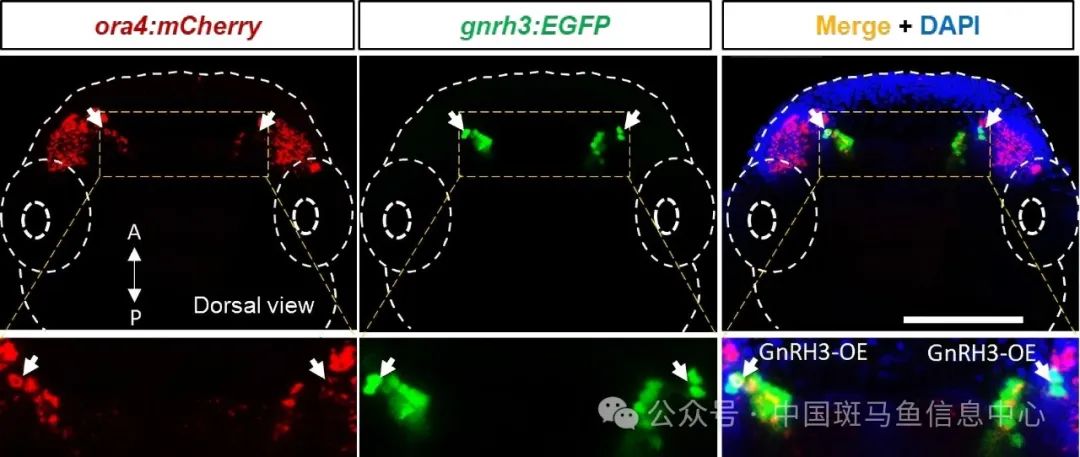
图2 斑马鱼GnRH3神经元是隐窝嗅觉感觉神经元
采用基因编辑技术将gnrh3突变后,gnrh3突变雄鱼的GnRH3神经元放电频率降低,对PGF2α的响应能力严重受损,导致gnrh3突变雄鱼的求偶行为障碍、繁殖成功率显著下降,并且,gnrh3突变雄鱼与对照雄鱼竞争雌鱼的求偶能力显著减弱。当研究人员选择性去除嗅觉上皮的GnRH3神经元后,雄性斑马鱼对PGF2α失去反应,表明GnRH3神经元合成和分泌的GnRH3神经肽对于GnRH3神经元感知和传递嗅觉信号及调控求偶行为的功能不可或缺。
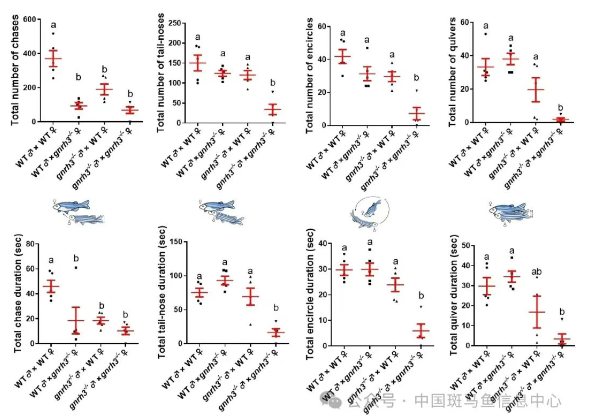
图3 gnrh3突变导致斑马鱼求偶行为障碍
研究表明,斑马鱼下丘脑外末端GnRH神经元兼具神经内分泌调控和直接感知环境性信息素信号的双重功能,揭示了GnRH神经元将化学信号转化为繁殖行为反应的神经通路,该机制可能也存在于其他脊椎动物,有望为人类生殖相关疾病(如卡尔曼综合征)和信息素感知相关行为研究提供启示。
水生所崔雪凡博士、陈露博士研究生和陶彬彬副研究员为论文共同第一作者,胡炜研究员、朱作言院士和Vance L. Trudeau教授为共同通讯作者。水生所段明研究员、罗大极研究员等参与研究工作,水生所分析测试中心给予技术支持。
该研究得到国家自然科学基金创新研究群体项目和渥太华大学国际合作等项目的资助。






